
Les cathodes à base de silicium stabilisent les cellules Li-S. Effet : plus de 2 cycles de charge au lieu de plusieurs dizaines
Des scientifiques de l'Institut des sciences et technologies de Daegu (DGIST, Corée du Sud) ont mis au point une cathode à base de silicium qui devrait résister à plus de 2 cycles de charge dans des cellules Li-S. Les cellules lithium-ion classiques utilisent du silicium pur dans les anodes pour compléter et remplacer progressivement le graphite. L'oxyde de silicium a été utilisé ici et le dioxyde de silicium a été utilisé dans la cathode.
Cellule Li-S = anode au lithium, cathode en dioxyde de silicium avec soufre
Les cellules Li-S sont considérées comme intéressantes en raison de leur densité énergétique élevée, de leur poids et de leur faible coût de fabrication. Cependant, personne n'a encore réussi à créer une version qui résisterait à plus de plusieurs dizaines de cycles de charge. Tout cela est dû aux polysulfures de lithium (LiPS), qui se dissolvent dans l'électrolyte lors de la décharge et réagissent avec l'anode, réduisant sa capacité et, par conséquent, détruisant la batterie.
Il est possible que des chercheurs sud-coréens aient trouvé une solution au problème. Au lieu de matériaux à base de carbone (comme le graphite), ils ont utilisé la cathode. structure lamellaire de la silice mésoporeuse (POMS).
La structure lamellaire est compréhensible, tandis que la mésoporosité fait référence à l'accumulation de pores (cavités) dans la silice qui ont une taille cible, une densité surfacique et une dispersion de petite taille (source). C'est un peu comme si vous poussiez régulièrement à travers des plaques adjacentes d'une sorte de silicate pour faire un tamis.
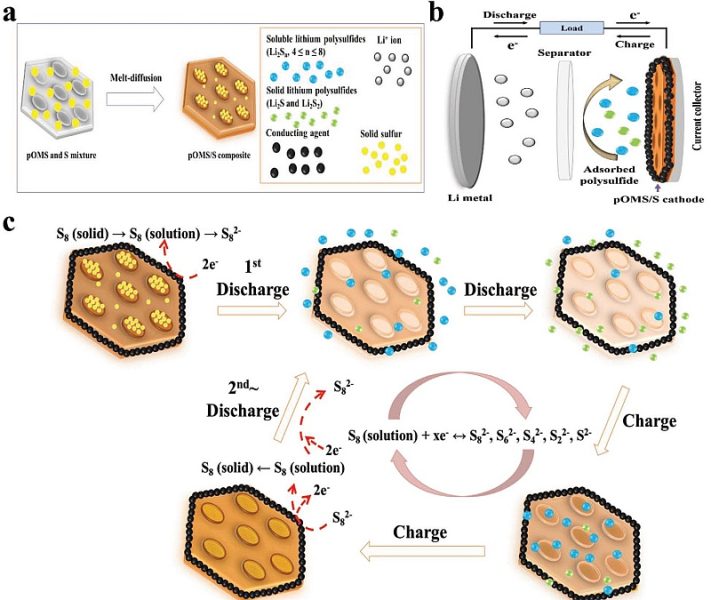
Les scientifiques de la DGIST ont utilisé ces trous pour y déposer du soufre (figure a). Lors de la décharge, le soufre se dissout et forme des polysulfures de lithium (LiPS) avec le lithium. Ainsi, la charge circule, mais le LiPS reste piégé près de la cathode en raison du facteur carbone supplémentaire non défini (structure noire, figure b).
Pendant la charge, LiPS libère du lithium, qui est renvoyé à l'anode de lithium. D'autre part, le soufre est converti en silice. Aucune fuite de LiPS à l'anode, aucun dommage au métal.
La batterie Li-S ainsi créée conserve une capacité et une stabilité élevées pendant plus de 2 cycles de travail. Au moins 500 à 700 cycles de fonctionnement sont considérés comme standard pour les cellules Li-ion classiques, bien qu'il faille ajouter que les cellules lithium-ion bien traitées peuvent supporter plusieurs milliers de cycles.
Cela peut vous intéresser :