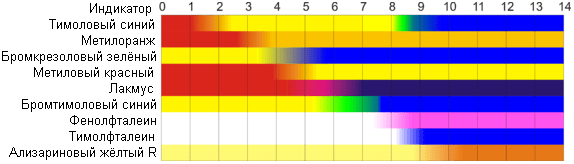
Indicateurs de pH naturels
Sous l'influence de changements dans la réaction de l'environnement, non seulement les composés utilisés dans les laboratoires comme indicateurs acquièrent des couleurs différentes. Un groupe tout aussi nombreux est constitué de substances contenues dans des produits naturels. Dans plusieurs essais, nous testerons le comportement des indicateurs de pH dans notre environnement.
Pour les expériences, plusieurs solutions avec des pH différents seront nécessaires. Ils peuvent être obtenus en diluant de l'acide chlorhydrique avec du HCl (une solution à pH 3-4% est de 0) et une solution d'hydroxyde de sodium NaOH (une solution à 4% a un pH de 14). L'eau distillée, que nous utiliserons également, a un pH de 7 (neutre). Dans l'étude, nous utiliserons du jus de betterave, du jus de chou rouge, du jus de myrtille et de l'infusion de thé.
Dans des éprouvettes contenant des solutions préparées et de l'eau distillée, déposer un peu de jus de betterave rouge (photographie 1). Dans les solutions acides, il acquiert une couleur rouge intense, dans les solutions neutres et alcalines, la couleur devient brune, se transformant en une teinte jaune (photographie 2). La dernière couleur est le résultat de la décomposition du colorant dans un environnement fortement alcalin. La substance responsable de la décoloration du jus de betterave est la bétanine. L'acidification du bortsch ou de la salade de betteraves est une « frite » culinaire qui donne au plat une couleur appétissante.
De la même manière, essayez le jus de chou rouge (photographie 3). Dans une solution acide, le jus devient rouge vif, dans une solution neutre, il devient violet clair et dans une solution alcaline, il devient vert. Dans ce cas également, la base forte décompose le colorant - le liquide dans le tube à essai devient jaune (photographie 4). Les substances qui changent de couleur sont les anthocyanes. Saupoudrer la salade de chou rouge de jus de citron lui donne un aspect attrayant.
Une autre expérience nécessite du jus de myrtille (photographie 5). La couleur rouge-violet vire au rouge en milieu acide, au vert en milieu alcalin et au jaune en milieu fortement alcalin (décomposition du colorant) (photographie 6). Ici aussi, les anthocyanes sont responsables de la modification de la couleur du jus.
L'infusion de thé peut également être utilisée comme indicateur de pH de la solution (photographie 7). En présence d'acides, la couleur devient jaune paille, en milieu neutre elle devient marron clair et en milieu alcalin elle devient marron foncé (photographie 8). Les dérivés du tanin sont responsables de la modification de la couleur de l'infusion, donnant au thé son goût acidulé caractéristique. L'ajout de jus de citron rend la couleur de l'infusion plus claire.
Il est également utile d'effectuer indépendamment des tests avec d'autres indicateurs naturels - de nombreux jus et décoctions de plantes changent de couleur en raison de l'acidification ou de l'alcalinisation de l'environnement.
A voir en vidéo :
Indicateurs de pH naturels
